原创 给细胞装“稳压器”!韩国科学家破解生物噪声,终结癌症耐药难题
文 | 钱钱
编辑 | 阿景
癌症复发和抗生素耐药性,这俩难题医生们头疼好多年了。

明明用了药,癌细胞杀不干净,细菌也总能变出耐药的“变种”,到底为啥?最近科学界有个新发现,可能把这俩问题的老底给揭了细胞里的“生物噪声”。
别被“噪声”这词唬住,说白了就是细胞里的蛋白质表达会随机波动。

就像同一个班的学生,都是一个老师教的,考试分数还是有高有低,细胞也这样,就算基因一样,干活的“蛋白质产量”也能差出一大截。
以前研究细胞,科学家总喜欢看“平均分”,觉得一群细胞的表现差不多就行。
直到20世纪末单细胞测序技术出来,才发现单个细胞的差异大着呢。
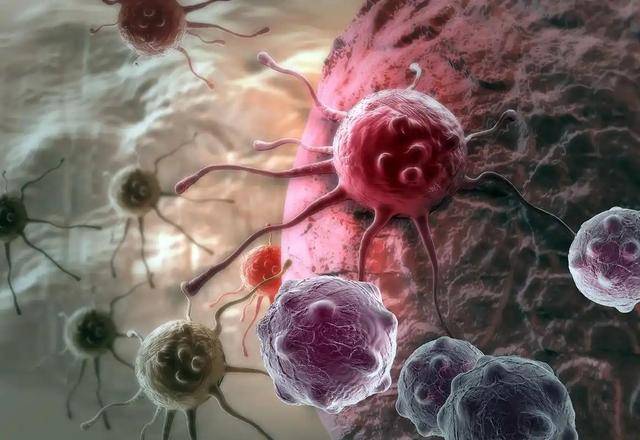
1998年有科学家用绿色荧光蛋白追踪单个细胞,第一次直观看到这种“不整齐”,原来细胞也有“调皮捣蛋”的个体。
细胞“调皮”也不全是坏事。
比如细菌遇到恶劣环境,部分细胞会通过噪声提前进入休眠状态,相当于留了个“后手”,等环境好了再“复活”。
这种随机波动,其实是生物进化出来的生存智慧。

但到了治病的时候,这种“调皮”就成了大麻烦。
化疗药杀癌细胞,大部分细胞都扛不住,但总有几个“刺头”因为蛋白质表达异常,耐药蛋白特别多,硬是扛过去了。
这些“漏网之鱼”就是后来复发的种子。
抗生素对付细菌也是一个道理,总有少数细菌靠噪声躲过去,慢慢变成耐药菌株。
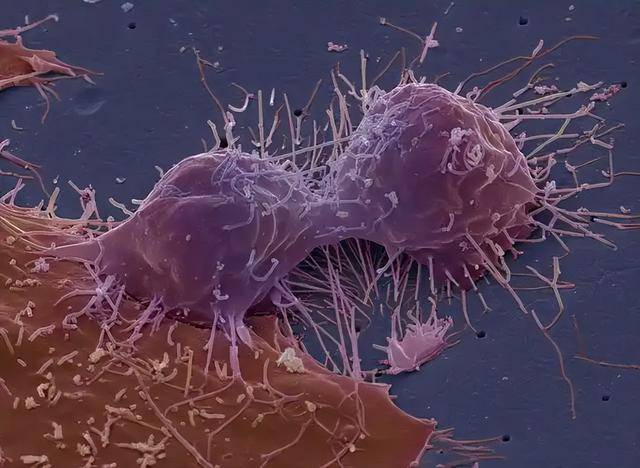
传统治疗手段拿这些“刺头”细胞没啥办法。
就说基因编辑或者药物干预吧,顶多能控制细胞群体的平均蛋白水平,反而可能让个体差异更大。
这就像调淋浴水温,你设定40℃,结果一会儿烫得跳脚,一会儿冻得发抖,极端情况根本管不住。
韩国科学技术院和浦项科技大学的团队搞出个新东西“噪声控制器”数学模型,说不定能把这些“叛逆”细胞给管明白。
这模型不是造新药,也不是改基因,而是从数学上想办法,让细胞的蛋白质表达“整齐划一”。
他们从工程控制论里找灵感,搞了个“鲁棒控制”模型。
简单说,就是给细胞装个“传感器”和“驱动器”。
传感器负责监测蛋白质水平波动,一旦发现哪个细胞“太跳”,驱动器就赶紧把多余的蛋白降解掉,形成闭环调控。
这个模型牛在哪儿?它把生物噪声压缩到了物理极限。
有个叫“法诺系数”的指标,专门衡量噪声大小,1是理论最低值。
他们用大肠杆菌做实验,正常情况下,DNA损伤后差不多五分之一的细胞会死掉,用了这个模型,蛋白水平统一了,死亡率降到了7%,存活率提升了快两倍。
以前生物反馈系统都是“被动响应”,比如细菌的乳糖操纵子,环境变了才跟着调整。

这个噪声控制器不一样,它能“主动预测”波动,提前出手调节,有点像给细胞配了个“智能管家”。
从实验室到病房,这个模型的应用前景挺让人期待。
就说癌症治疗吧,要是能控制肿瘤细胞里耐药蛋白的噪声,把那些“极端耐药细胞”都干掉,化疗药就能均匀作用于所有癌细胞,从根上断了复发的路。
而且不用开发新药,把控制器元件装到病毒载体里,靶向送到肿瘤细胞就行,转化起来相对容易。

合成生物学领域也等着它救命呢。
现在用工程菌株生产胰岛素、疫苗,产量波动能差出一半,就是因为细胞表达噪声太大。
要是用这个模型把蛋白水平统一了,产量稳定下来,生物制造的效率能提一大截。
当然,从理论到实际应用还有坎要过。
真实细胞里的代谢网络乱七八糟,传感器和驱动器可能被其他信号干扰。
团队说下一步要把模型变成实际的基因回路,先在酵母和哺乳动物细胞里试试水,争取3-5年内搞出实验室原型。
这个研究最让人兴奋的不是某个具体技术,而是它的思路。

以前咱们总觉得生物系统的随机性是没办法的事,现在用数学工具一梳理,居然能主动调控了。
这就像人类第一次学会给生命系统“写代码”,以后设计细胞行为,可能就像工程师设计机器一样精准。
要是这个模型真能落地,10年内说不定就能用到临床上。
到时候癌症复发、抗生素耐药这些老大难,可能就真成了历史。
科学这东西就是这样,有时候换个角度看问题,老难题突然就有了新解。
细胞那些“小脾气”,以后终于有人能管得住了。
